关于细胞力学在肿瘤恶性肿瘤中的作用的新见解
癌症作为一种威胁生命的疾病,一直是研究的重点。了解肿瘤进展的机制一直是一个重大挑战。近年来,越来越多的证据表明肿瘤细胞的机械特性与肿瘤进展和恶性肿瘤之间存在相关性。
然而,肿瘤细胞力学与恶性肿瘤之间的关系仍不完全清楚。为了弥补这一知识空白,香港理工大学谭友华博士的团队发现了肿瘤细胞力学在恶性肿瘤中的调节作用,并揭示了其潜在机制。
Tan 博士的研究表明,通过靶向肌动蛋白细胞骨架和肌球蛋白活性,肿瘤细胞的适度软化增强了它们的自我更新和肿瘤形成能力,而细胞硬化则抑制了各种类型癌症的这些能力。
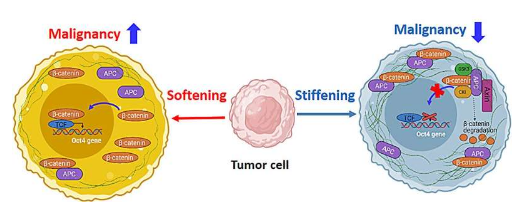
从机制上讲,肌动蛋白细胞骨架的软化/硬化减弱/加强了抑癌腺瘤性结肠息肉病 (APC) 和 β-连环蛋白之间的相互作用,导致 β-连环蛋白定位于核/细胞质。
核定位的β-连环蛋白与Oct4基因的启动子区域结合,促进关键基因转录并维持肿瘤细胞的自我更新能力。相反,β-连环蛋白的细胞质滞留导致其降解并随后导致 Wnt/β-连环蛋白信号失活,从而降低肿瘤细胞的干性。
此外,细胞力学调节肿瘤干细胞和非肿瘤干细胞之间的相互转化,这一过程依赖于 Wnt 信号传导。总之,本研究证明肌动球蛋白介导的细胞力学通过细胞骨架/APC/Wnt/β-catenin/Oct4信号通路驱动肿瘤细胞的自我更新和肿瘤形成能力。这些发现已得到临床验证,并与癌症患者的生存显着相关。
这项研究的发现为深入了解肿瘤进展提供了新的视角,并为开发针对肿瘤细胞力学的新治疗方法提供了重要线索。这项研究首次证明,肿瘤细胞在进展过程中软化不仅是肿瘤进化的结果,也是肿瘤发展的关键驱动力。
这项研究为开发用于癌症预防和治疗的新机械医学开辟了新途径。
免责声明:本答案或内容为用户上传,不代表本网观点。其原创性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容、文字的真实性、完整性、及时性本站不作任何保证或承诺,请读者仅作参考,并请自行核实相关内容。 如遇侵权请及时联系本站删除。
